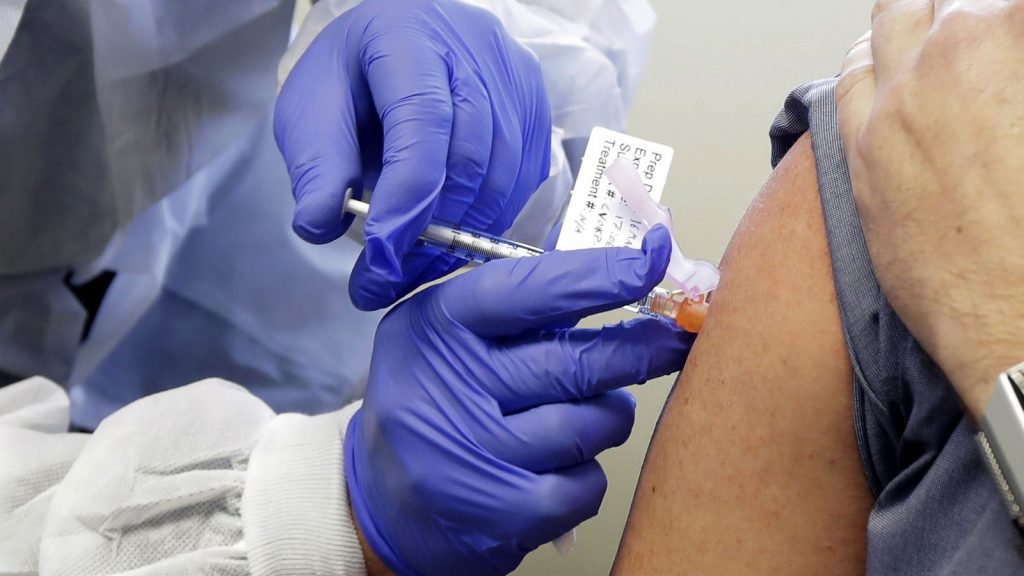
Durante la mañana de este lunes, la farmacéutica Pfizer afirmó que su vacuna contra la Covid-19 es eficaz en un 90%, dato que se obtuvo tras publicar los resultados del primer análisis intermedio de su ensayo de fase 3, última etapa antes de pedir formalmente su homologación.
En un comunicado presentado por la farmacéutica estadounidense en conjunto con la firma BioNtech, se indicó que la eficacia de protección frente al virus SARS-CoV-2 se logró siete días después de la segunda dosis de vacuna y 28 días después de la primera.
Es así que, según las proyecciones actuales, la empresa espera producir a nivel mundial hasta 50 millones de dosis de vacunas en 2020 y hasta 1.300 millones de dosis en 2021.
Sin embargo, en Chile, el acuerdo involucra a 10,1 millones de dosis, avance que fue destacado este lunes por el Presidente de la República, Sebastián Piñera, quien señaló “Esperamos poder iniciar nuestro programa de vacunación durante los primeros meses del próximo año. Ya tenemos los contratos firmados”.
DATOS RELEVANTES
El ensayo clínico de fase 3 que comenzó el 27 de julio, ha inscrito a 43.538 participantes hasta la fecha, cifra de la cual el 42% de los participantes globales y el 30% de los estadounidenses tienen antecedentes raciales y étnicos diversos. Además 38.955 personas recibido una segunda dosis de la vacuna candidata al 8 de noviembre.
No obstante, continúan las inscripciones a la prueba y se espera que continúe hasta el análisis final cuando se hayan acumulado un total de 164 casos confirmados de Covid-19, ya que el estudio también evaluará el potencial de la vacuna en aquellos que han tenido una exposición previa al SARS-CoV-2, así como su prevención contra casos graves.
Por otra parte, la presentación de la autorización de uso de emergencia a la Administración de Alimentos y Medicamentos de los EE. UU. (FDA) está prevista para poco después que se alcance el hito de seguridad requerido, que actualmente se espera que ocurra en la tercera semana de noviembre.
Actualmente, Pfizer y BioNTech son los primeros en publicar el resultado del análisis intermedio de la fase tres, pero según la Organización Mundial de la Salud (OMS), existen además otros nueve proyectos de vacuna en el mundo que se hallan en la misma etapa, como la farmacéutica estadounidense Moderna, varios laboratorios estatales de China y la Universidad de Oxford asociada con AstraZeneca.
APROBACIÓN DE EMERGENCIA PARA CHILE
Respecto a la situación, el ministro de Salud, Enrique Paris, se refirió a la vacuna y comentó que “Esta vacuna ha sido probada en más de 43 mil personas. Eso ya da un margen también de bastante… un estudio bastante bien hecho y se va a solicitar, como se ha definido también en Chile, una aprobación de emergencia para usar la vacuna”.
¿Cuándo se podría solicitar esto?
Según Paris, esto podría darse cuando por ejemplo en un país hay una situación de pandemia como la que está viviendo el mundo, y “esta solicitud de emergencia, para que quede claro, tiene que aceptarla, en el caso de Chile, el Instituto de Salud Pública. En el caso de Estados Unidos, la FDA, etc”, indicó.
¿Cuándo se podría implementar en Chile?
Respecto a una posible compra e importación de vacunas y su tiempo estimado, el ministro de Salud, señaló que en primer lugar la vacuna debe ser aprobada por la FDA, ya que es una vacuna americana.
Posteriormente, como el Instituto de Salud Pública (ISP) nacional tiene categoría 4, puede aceptar esa aprobación de otra agencia de la misma categoría para poder aplicar la vacuna en Chile, es decir “no sería necesario hacer nuevas pruebas en Chile para poder aprobar la vacuna”, según palabras del ministro.
Asimismo, señaló ciertas condiciones que se deben considerar, ya que “esta vacuna es una vacuna nueva que requiere de dos dosis. Debe mantenerse a una temperatura bastante más baja que lo que habitualmente usan otro tipo de vacunas, por lo tanto, la estrategia y la planificación para colocarla tiene que ser muy cuidadosa y después de la segunda dosis se ha logrado en los sujetos que han recibido parte, o participado en el estudio, una protección del 90%, que se logra justamente siete días después de la segunda dosis”, explicó.